幽门螺杆菌(Helicobacter pylori)感染是全球最常见的慢性细菌感染之一,约半数人口受其影响,与慢性胃炎、胃溃疡甚至胃癌密切相关。目前,临床治疗幽门螺杆菌仍主要依赖抗生素方案。然而,胃部强酸环境、胃黏液屏障以及胃蠕动等因素会显著降低药物在胃部的有效浓度,导致治疗失败率较高,并可能引发肠道菌群失衡及抗生素耐药问题。
2026年1月27日,西南大学赵萍教授团队在国际权威期刊《Journal of Nanobiotechnology》(中科院一区Top,IF=12.6)在线发表了题目为《Silk-based biomimetic nanocomposite for precision eradication of Helicobacter pylori and gut microbiome preservation》的研究论文。该研究开发出一种基于仿生蚕丝材料的纳米复合递药系统,能够在胃部实现精准定位与持续释放抗生素,从而显著提高幽门螺杆菌清除效率,同时减少对肠道菌群的影响。

仿生策略:从细菌黏附机制获得灵感
幽门螺杆菌之所以能在胃部长期定植,与其表面黏附素蛋白(BabA、SabA)能够特异识别并结合于胃粘膜上皮细胞糖链结构密切相关。研究团队受这一机制启发,将细菌黏附素蛋白结构域与蚕丝蛋白进行融合,构建出两种黏附素丝素融合蛋白——SF-BAR 和 SF-SAR。通过转基因家蚕丝腺表达系统,成功在蚕丝中合成了这两种功能蛋白,并利用其制备出具有黏附能力的丝素纳米颗粒(BS-NPs)。这些纳米颗粒能够模拟幽门螺杆菌的黏附行为,更容易与胃黏膜细胞结合,从而实现在胃部的精准定位与长时间滞留。结合具有流动性的丝素水凝胶载体(FSF-Gel)包裹纳米粒,构建完整的药物递送系统 BSNG,提供保护屏障防止胃酸破坏,并凭借粘附性和剪切变稀特性覆盖胃黏膜,实现药物胃局部持续释放。
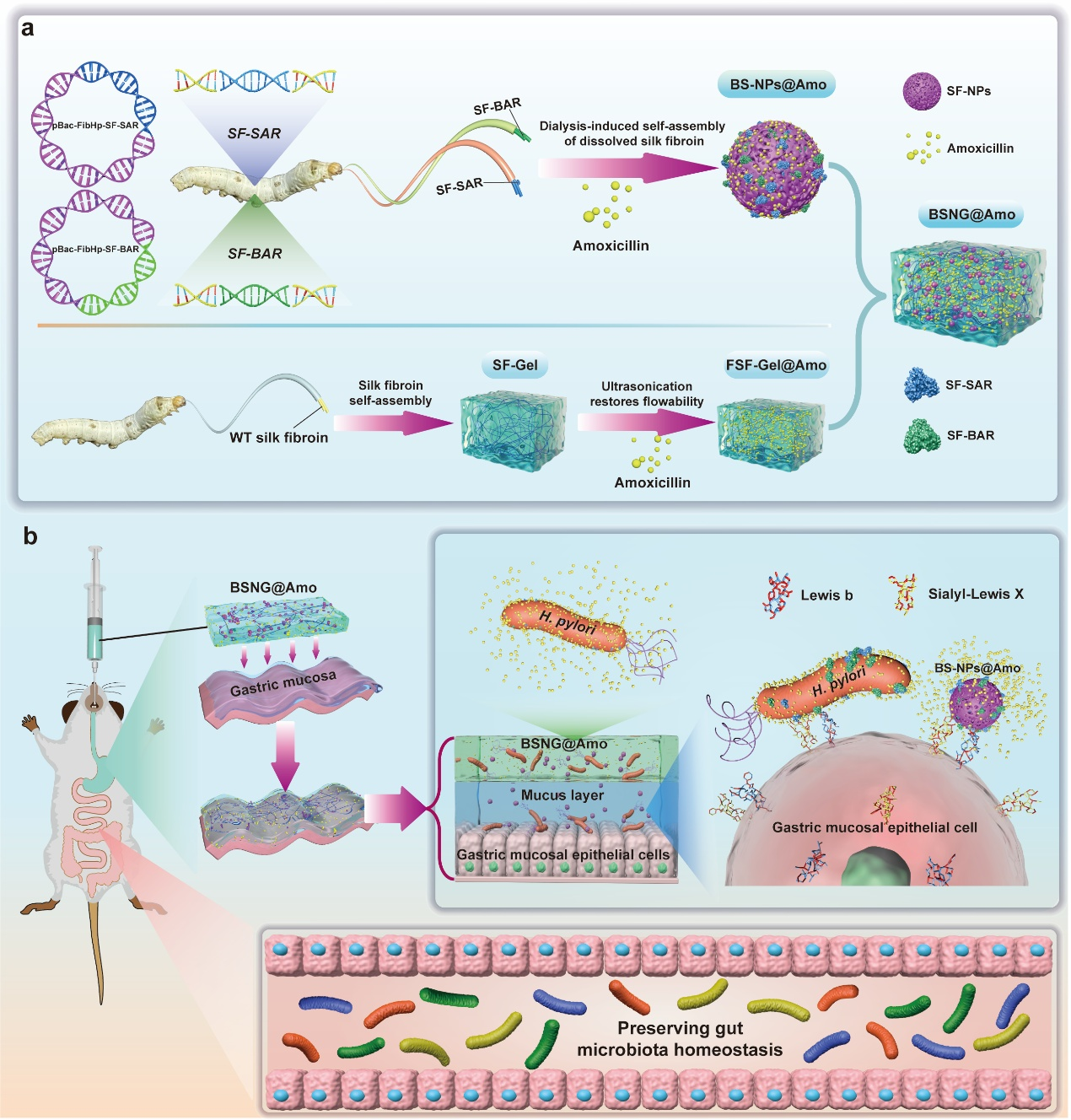
精准杀菌,同时保护肠道菌群
研究结果表明,BSNG 系统递送的阿莫西林能够显著提高胃组织中的局部药物浓度,对幽门螺杆菌的清除效果明显优于传统给药方式。在降低给药频率的情况下仍能保持良好疗效。同时,药物主要在胃部局部释放作用,从而有效降低对肠道微生物群的干扰,减少传统抗生素治疗可能引发的菌群失衡问题。
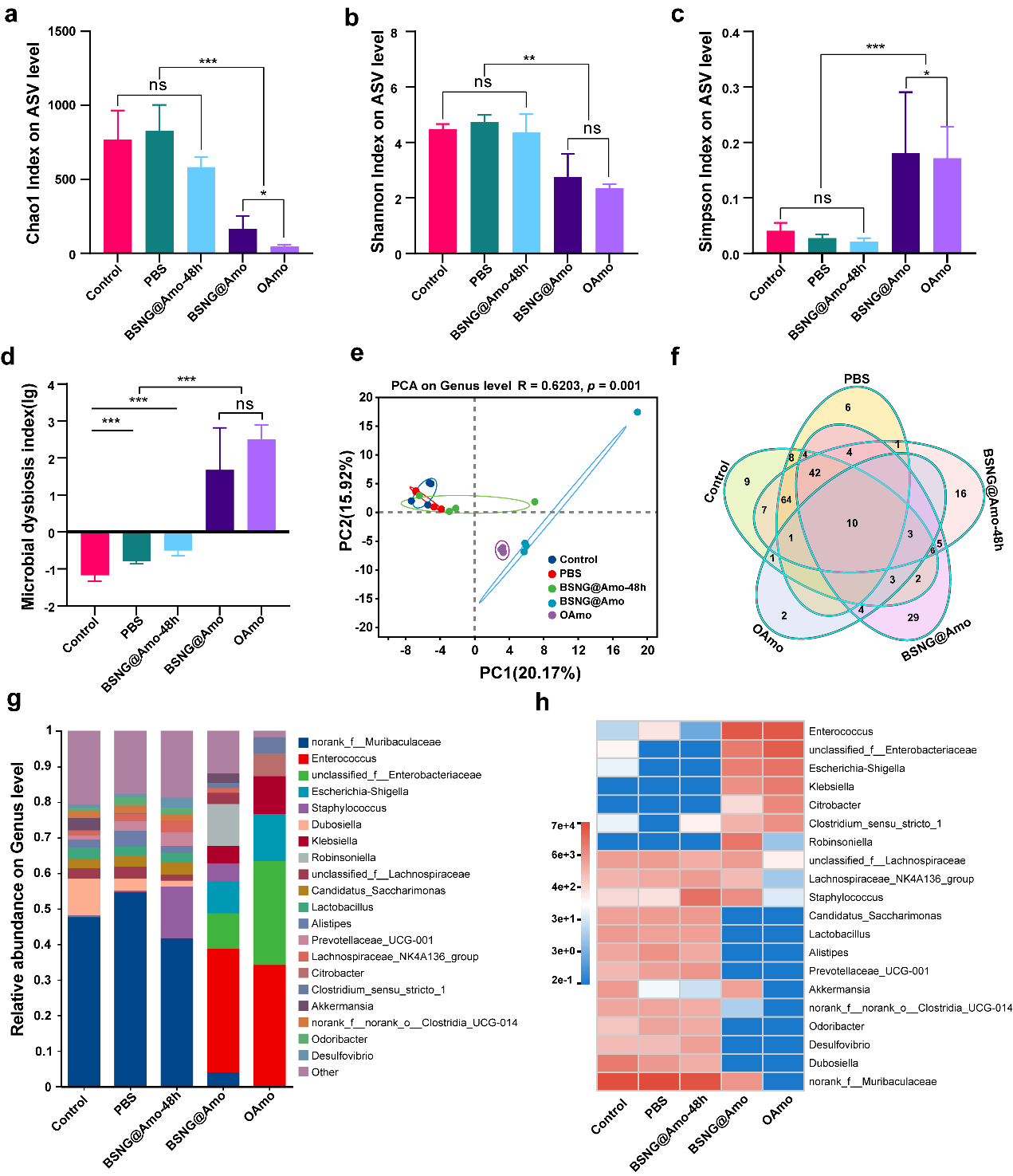
蚕丝材料的跨界潜力
丝素蛋白来源于天然蚕丝,具有良好的生物相容性、可降解性和结构可设计性,已在组织工程和药物递送等领域广泛应用。本研究进一步展示了基因工程蚕丝材料在精准医疗中的应用潜力。通过在分子层面引入功能结构域,可赋予丝素材料新的生物功能。总体而言,该研究构建了一种仿生、精准且长效的胃部抗菌递药平台,可在胃部定向释放抗生素,高效清除幽门螺杆菌并减少对肠道菌群的影响,为胃部疾病精准治疗提供了新的策略。
西南大学前沿交叉学科研究院生物学研究中心博士研究生黄光成为论文第一作者。赵萍教授为论文最后通讯作者,夏庆友教授为论文共同通讯作者。本研究得到国家重点研发计划(2022YFD1201600)和国家自然科学基金(32030103、32172798)的资助。